GD-150 : Conception et mise en oeuvre d'un programme d'essais biologiques
Préface
Le présent document d'orientation de la réglementation aide à concevoir et à mettre en œuvre un programme d'essais biologiques, conformément à la Loi sur la sûreté et la réglementation nucléaires (LSRN) et à ses règlements.
Ce document d'orientation présente les concepts fondamentaux permettant d'établir la nécessité d'un programme d'essais biologiques, de choisir les participants et de fixer la fréquence d'échantillonnage optimale. Il propose également des méthodes visant à interpréter les résultats.
Les principes et éléments clés de l'élaboration du présent guide sont conformes aux normes, guides, et recommandations, nationales et internationales, notamment les documents DOE Standard Internal Dosimetry (DOE-Std-1121-98), du U.S. Department of Energy; l'American National Standard-Design of Internal Dosimetry Programs (ANSI/HPS N13.39-2001) de la Health Physics Society; et le Guide de sûreté RS-G-1.2, Évaluation de l'exposition professionnelle due à l'incorporation de radionucléides, de l'Agence internationale de l'énergie atomique (AIEA).
Aucun élément contenu dans ce guide ne doit être interprété par le titulaire de permis comme une autorisation de déroger aux exigences des règlements pertinents. Le titulaire de permis a la responsabilité d'identifier la législation, les conditions de permis, les lignes directrices ou les normes applicables et d'y adhérer.
Table des matières
- 1.0 Introduction
- 2.0 Programmes et choix des participants
- 3.0 Méthode et fréquence des essais biologiques
- 4.0 Interprétation des résultats
- 5.0 Enregistrement des résultats d'essais biologiques
- Annexe A : Choix des participants à un programme d'essais biologiques courants basé sur l'activité manipulée
- Annexe B : Exemples
- B.1 Exemple 1 : Détermination de la participation à un programme d'essais biologiques
- B.2 Exemple 2 : Détermination de l'erreur de comptage (incertitude)
- B.3 Exemple 3 : Détermination de la fréquence de surveillance des incorporations de 137Cs
- B.4 Exemple 4 : Détermination de la fréquence de surveillance des incorporations de 131I
- B.5 Exemple 5 : Niveaux d'enquête dérivés pour l'inhalation de 137Cs
- Glossaire
- Références
- Renseignements Additionnels
1.0 Introduction
1.1 Objet
Le présent document d'orientation d'application de la réglementation aide à concevoir et à mettre en oeuvre un programme d'essais biologiques, conformément à la Loi sur la sûreté et la réglementation nucléaires (LSRN, la Loi) et à ses règlements.
1.2 Portée
Le document d'orientation de la réglementation présente les concepts fondamentaux permettant d'établir la nécessité d'un programme d'essais biologiques, de choisir les participants et de fixer la fréquence d'échantillonnage optimale. Il propose également les méthodes d'interprétation et d'enregistrement des résultats.
1.3 Dispositions législatives applicables
Les dispositions de la LSRN et des règlements connexes à la LSRN qui s'appliquent au présent guide sont les suivants :
- L'article 27 de la LSRN, qui stipule que « les titulaires de licence ou de permis et les personnes visées par règlement : a) tiennent les documents réglementaires, notamment un document sur la quantité de rayonnement reçue par chaque personne—ou la dose engagée à l'égard de chaque personne—dont les fonctions professionnelles sont liées aux activités autorisées par la présente loi ou qui se trouve dans un lieu où celles-ci sont exercées, les conserve durant la période réglementaire… »
- L'alinéa 3(1)e) du Règlement général sur la sûreté et la réglementation nucléaires, qui stipule que « la demande de permis comprend les renseignements suivants : …e) les mesures proposées pour assurer l'observation du Règlement sur la radioprotection… »
- L'article 28 du Règlement général sur la sûreté et la réglementation nucléaires, qui stipule que :
« (1) La personne qui est tenue de conserver un document aux termes de la Loi, de ses règlements ou d'un permis, le fait pour la période indiquée dans le règlement applicable ou, à défaut, pendant une année suivant l'expiration du permis qui autorise l'activité pour laquelle les documents sont conservés.
« (2) Il est interdit à quiconque d'aliéner un document mentionée dans la Loi, ses règlements ou un permis à moins : a) de ne plus être tenu de le conserver aux termes de la Loi, de ses règlements ou du permis; b) de donner à la Commission un préavis d'au moins 90 jours indiquant la date d'aliénation et la nature du document.
« (3) La personne qui avise la Commission conformément au paragraphe (2) dépose l'original ou une copie du document auprès d'elle sur demande » - Le paragraphe 1(2) du Règlement sur la radioprotection, qui stipule que « pour l'application de la définition de « service de dosimétrie » à l'article 2 de la Loi, est désignée un service de dosimétrie l'installation servant à la mesure et au contrôle des doses de rayonnement reçues par un travailleur du secteur nucléaire, ou engagées à son égard, lorsque le travailleur au cours d'une période de dosimétrie d'un an, risque vraisemblablement de recevoir une dose efficace supérieure à 5 mSv »
- Le paragraphe 1(3) du Règlement sur la radioprotection, qui stipule que « pour l'application de la définition de « travailleur du secteur nucléaire » à l'article 2 de la Loi, la limite fixée pour la population est de 1 mSv par année civile »
- L'alinéa 4a) du Règlement sur la radioprotection, qui stipule que « le titulaire de permis met en œuvre un programme de radioprotection et, dans le cadre de ce programme : a) maintient (…) la dose efficace et la dose équivalente qui sont reçues par la personne, et engagées à son égard, au niveau le plus bas qu'il soit raisonnablement possible d'atteindre, compte tenu des facteurs économiques et sociaux, par : … iii) le contrôle de l'exposition du personnel et du public au rayonnement, »…
- Le paragraphe 5(1) du Règlement sur la radioprotection, qui stipule que « pour tenir le document sur les doses de rayonnement prévu à l'article 27 de la Loi, le titulaire de permis contrôle et enregistre (…) la dose efficace et la dose équivalente qui sont reçues par la personne et engagées à son égard »,
- Le paragraphe 5(2) du Règlement sur la radioprotection, qui stipule que « le titulaire de permis contrôle (…) la dose efficace et la dose équivalente : a) par mesure directe résultant du contrôle; b) par évaluation, lorsque le temps et les ressources exigés pour une mesure directe sont trop importants par rapport à son utilité »,
- L'article 8 du Règlement sur la radioprotection, qui stipule que « le titulaire de permis utilise un service de dosimétrie autorisé pour mesurer et contrôler les doses de rayonnement reçues par le travailleur du secteur nucléaire, et engagées à son égard, lorsque le travailleur risque vraisemblablement de recevoir une dose efficace supérieure à 5 mSv au cours d'une période de dosimétrie d'un an »,
- L'article 19 du Règlement sur la radioprotection, qui stipule que « le titulaire de permis qui exploite un service de dosimétrie dépose au Fichier dosimétrique national du ministère de la Santé, à la fréquence prévue dans le permis et sous une forme compatible avec le Fichier, les renseignements suivants à l'égard de chaque travailleur du secteur nucléaire pour qui le service a mesuré et contrôlé une dose de rayonnement :
- les prénoms, le nom de famille et tout nom de famille antérieur du travailleur;
- le numéro d'assurance sociale du travailleur;
- le sexe du travailleur;
- la catégorie d'emploi du travailleur;
- la date, la province et le pays de naissance du travailleur;
- le degré d'exposition du travailleur aux produits de filiation du radon
- la dose efficace et la dose équivalente reçues par le travailleur et engagées à son égard »,
- L'article 24 du Règlement sur la radioprotection, qui stipule que « le titulaire de permis tient un document contenant les nom et catégorie d'emploi de chaque travailleur du secteur nucléaire. »
2.0 Programmes et choix des participants
L'objectif principal d'un programme d'essais biologiques est d'assurer la sécurité des travailleurs et d'évaluer la charge corporelle reçue par un travailleur suite à l'exposition à des radionucléides.
Les principaux composants d'un programme d'essais biologiques sont les critères de participation au programme, la fréquence de la surveillance et les mesures à prendre en fonction des résultats des mesures.
Quatre types de programmes d'essais biologique sont décrits dans cette section : les essais biologiques de référence, les essais biologiques courants, les essais biologiques spéciaux, et les essais de confirmation. La Section 3.0, Méthode et fréquence des essais biologiques et la Section 4.0, Interprétation des résultats décrivent la fréquence des essais et l'interprétation des résultats.
2.1 Essai biologique de référence
L'essai biologique de référence consiste à évaluer la charge corporelle reçue antérieurement par un travailleur suite à son exposition à des radionucléides. Le type d'essai de référence effectué dépend du type de radionucléides pour lequel le travailleur fait régulièrement l'objet de contrôles. L'essai biologique de référence devrait être effectué en début d'emploi, ou avant de réaliser des travaux exigeant des essais biologiques courants. Cet essai permet de déterminer l'exposition aux radionucléides reçue antérieurement par le travailleur lors de ses expériences de travail précédentes, ou lors de procédures médicales, et de déterminer la charge corporelle naturelle (cette charge corporelle contribue au rayonnement de fond).
Les radionucléides qui ne peuvent pas faire l'objet d'essais biologiques, comme le radon et les produits de filiation du radon, sont surveillés par échantillonnage d'air. Cependant, il convient de noter que l'essai biologique de référence a pour but d'évaluer la quantité de radionucléides dans le corps d'un travailleur résultant d'incorporations survenues avant que le travailleur ne débute l'emploi. L'échantillonnage de l'air en milieu de travail ne fournit pas cette information. Lorsque la surveillance de l'air des lieux de travail est le seul moyen d'évaluer les incorporations de radionucléides, l'essai biologique de référence n'est pas effectué. Il peut être requis d'obtenir l'information concernant les incorporations antérieures auprès de l'employeur précédent. [1]
La réalisation d'un essai de référence ne signifie pas que des mesures de référence seront effectuées. L'examen administratif des antécédents du travalleur peut mener à la conclusion que des mesures de référence ne sont pas requises, parce que les résultats attendus sont déjà prévisibles (par exemple, aucune activité détectable, ou aucun antécédent d'exposition). Un tel examen peut constituer une évaluation acceptable des données de référence. [1]
La réalisation d'un essai biologique de référence est appropriée dans les cas suivants : [1, 2]
- Le travailleur a déjà été exposé aux radionucléides pertinents et la rétention efficace par le corps pourrait dépasser l'activité dérivée;
- L'information sur les antécédents d'exposition n'est pas disponible, ou ceux-ci sont non concluants;
- Le travailleur travaillera avec des substances nucléaires radioactives qui pourraient être détectables dans le cadre d'essais biologiques et attribuables à des sources autres que les sources en milieu de travail.
2.2 Essais biologiques courants
Les doses associées à l'incorporation de radionucléides devraient être évaluées pour tous les travailleurs qui risquent vraisemblablement de recevoir une dose efficace engagée (DEE) supérieure à 1 mSv par année. Ces travailleurs sont désignés comme étant des travailleurs du secteur nucléaire (TSN).
Dans les cas où il est peu probable que le travailleur reçoive une dose annuelle dépassant 1 mSv, il pourrait être difficile de justifier le coût de la réalisation d'essais biologiques courants. Dans ce cas, la dose peut être évaluée par une estimation; par exemple, en effectuant une surveillance en milieu de travail. [3]
Le titulaire de permis devrait identifier quels sont les travailleurs qui risquent vraisemblablement de recevoir :
- Une dose efficace annuelle engagée (c.-à-d. somme de toutes les doses provenant d'une incorporation de radionucléides en milieu de travail sur une période d'un an) pouvant aller jusqu'à 1 mSv (travailleurs autres que les TSN);
- Une dose efficace annuelle engagée supérieure à 1 mSv et une dose efficace annuelle totale (c.-à-d. somme de toutes les doses efficaces annuelles provenant de sources externes et de la dose efficaces annuelle engagée) pouvant aller jusqu'à 5 mSv (TSN participant à un programme d'essais biologiques courants, pas nécessairement offert par un service de dosimétrie autorisé);
- Une dose efficace annuelle engagée supérieure à 1 mSv et une dose efficace annuelle totale supérieure à 5 mSv (TSN participant à un programme d'essais biologiques courants offert par un service de dosimétrie autorisé). [Règlement sur la radioprotection, article 8]
La probabilité que la limite de 1 mSv par année soit dépassée peut être évaluée en fonction de l'activité manipulée par le travailleur, le type de radionucléides en cause, la forme physique et chimique des radionucléides, le type de confinement utilisé et la nature des opérations effectuées. Lorsqu'un type de radionucléide est manipulé chaque jour (c.-à-d. environ 250 jours par année), les travailleurs qui manipulent des radionucléides dont l'activité figure au tableau 1 devraient participer à un programme d'essai biologique. Il convient de noter que, pour décider de la participation du travailleur au programme, les résultats des essais biologiques devraient remplacer les données du tableau 1.
Les fondements sur lesquels reposent les valeurs présentées au tableau 1 sont expliqués dans l'annexe A,Choix des participants à un programme d'essais biologiques courants basé sur l'activité manipulée, et l'on peut s'en servir pour dériver des valeurs propres au site. L'annexe A définit les paramètres requis pour définir la fraction d'incorporation potentielle (FIP). Pour un scénario d'incorporation particulier, la valeur LAI / FIP représente l'activité manipulée par jour de travail qui pourrait donner lieu à une incorporation annuelle égale à la limite annuelle d'incorporation (LAI), et, par conséquent, à une dose efficace engagée de 20 mSv par année. Le critère fixé pour la participation à un essai biologique est de 1 mSv. Par conséquent, les données figurant au tableau 1 représentent la quantité LAI / (20 * FIP).
Tableau 1 : Activité manipulée quotidiennement sur une période d'un an, au-delà de laquelle un essai biologique est recommandé
| Confinement | Volatilité | ||
|---|---|---|---|
| Gaz et liquides volatils | Poudres | Liquides non volatils et matières solides | |
| Aucun | ≥ 2 * LAI | ≥ 20 * LAI | ≥ 200 * LAI |
| Hotte | ≥ 200 * LAI | ≥ 2,000 * LAI | ≥ 20,000 * LAI |
| Boîte à gants | ≥ 20,000 * LAI | ≥ 200,000 * LAI | ≥ 2,000,000 * LAI |
| Pseudo-scellé | ≥ 50 * LAI | Not applicable | ≥ 10,000 * LAI |
Il est recommandé que les travailleurs qui doivent porter un équipement de protection respiratoire spécifiquement pour limiter l'incorporation de radionucléides fassent l'objet d'essais biologiques.
Les sources « pseudo-scellé» [4] sont des radionucléides à courte période qui sont manipulés exclusivement dans des flacons scellés et des seringues, et qui respectent les conditions suivantes :
- la période radiologique est inférieure à 7 jours;
- la manutention de la radioactivité est plus ou moins uniforme durant l'année;
- la matière radioactive n'est pas mise à l'état d'aérosol, ni portée à ébullition dans un contenant ouvert ou comportant des ouvertures;
- la matière radioactive se présente sous la forme d'une solution diluée;
- la matière radioactive est contenue dans un flacon multi-doses qui n'est jamais ouvert, et dont les quantités prédosées sont retirées uniquement au moyen de seringues en vue de l'injection immédiate dans un autre flacon multi-doses, ou dans un autre type de contenant fermé, ou administrée aux patients.
Les données du tableau 1 sont générales et n'englobent pas tous les scénarios. On suppose également qu'il y a des barrières mécaniques ou d'autres barrières physiques en place pour protéger le travailleur (comme des boîtes à gants et des hottes), que ces barrières sont appropriées pour le radioisotope manipulé, et qu'elles sont utilisées convenablement et entretenues de manière appropriée.
Lorsque plus d'un type de radionucléides sont manipulés, les étapes suivantes doivent être respectées afin de déterminer si le travailleur devrait participer à un programme d'essais biologiques :
- Calculer le ratio, rj, de la quantité d'un radionucléide, j, manipulé quotidiennement, à la quantité maximale de ce radionucléide pouvant être manipulée quotidiennement et au-delà de laquelle un essai biologique est recommandé, selon le tableau 1.
- Calculer ce rapport pour tous les autres radionucléides manipulés.
- Additionner tous les rapports calculés aux étapes 1 et 2 :
R = rj
Un essai biologique devrait être réalisé pour tous les radionucléides dont le rj ≥ 1; si R ≥ 1, un essai biologique devrait être réalisé pour tous les radionucléides pour lesquels le rj ≥ 0,3 [4, 5]. Dans les cas où R < 1, mais où n'importe laquelle des valeurs de rj est supérieure à 0,3, le titulaire de permis peut choisir d'assujettir le travailleur à un essai relativement à un radionucléide particulier. Un exemple de ce calcul figure à l'annexe B, Exemples, Exemple 1.
Un travailleur peut être retiré du programme d'essais biologiques s'il existe suffisamment de preuves à l'effet que l'incorporation en milieu de travail ne risque vraisemblablement pas de donner lieu à une dose dépassant 1 mSv par année. Il convient de fournir des preuves à l'appui, comme des résultats de surveillance de l'air.
2.3 Essais biologiques spéciaux
Les essais biologiques spéciaux sont réalisés suite à des circonstances particulières, comme des incorporations connues ou présumées de matières radioactives survenant dans des circonstances anormales (incident) sur les lieux de travail. Les essais biologiques sont souvent qualifiés comme étant des essais « ad-hoc » ou « ponctuels ». La surveillance relative aux essais biologiques spéciaux peut être déclenchée soit par un résultat de surveillance courante ou par un incident anormal laissant présumer qu'un seuil d'intervention (tel que défini dans le Règlement sur la radioprotection) ou que la limite de dose pourraient avoir été dépassés. Des directives relatives aux essais biologiques spéciaux sont données dans le document de la CCSN G-147, Protocoles d'intervention pour les essais biologiques en cas d'incorporation anormale de radionucléides [6].
2.4 Essais de confirmation
Le programme d'essais biologiques de confirmation a pour but : [1, 7, 8]
- de vérifier les hypothèses relatives aux conditions d'exposition radiologique sur les lieux de travail;
- de déterminer l'efficacité des mesures de radioprotection;
- de s'assurer que l'essai biologique courant n'est pas requis.
Cela peut comprendre la surveillance des lieux de travail ou une surveillance individuelle limitée des travailleurs qui ne correspond pas aux critères de participation à un programme d'essais biologiques. (à noter que l'expression « essai de confirmation » ne devrait pas être confondue avec l'expression « dépistage » qui est parfois utilisé en faisant allusion aux essais biologiques effectués lorsque les résultats sont inférieurs à l'activité dérivée (AD : décrite à la section 4.2, Mise en perspective des résultats des essais biologiques) et, par conséquent, la dose efficace engagée n'est pas évaluée.)
Lorsque des travailleurs manipulent des radionucléides non scellés ou qu'ils peuvent y être exposés, mais qu'ils ne satisfont pas aux critères de participation à un programme d'essais biologiques courants, la surveillance des incorporations peut être effectuée dans le cadre d'un programme de confirmation. La fréquence des essais peut être la même que la fréquence des essais courants, ou peut varier si l'exposition potentielle à des radionucléides non scellés est peu fréquente (en tenant compte de la période biologique des radionucléides).
Dans le cadre d'un programme de confirmation, le travailleur se soumet à des essais biologiques in vivo ou in vitro (voir section 3.1, Méthodes d'essais biologiques) et il peut être nécessaire d'échantillonner une fraction (p. ex. 10 % à 50 %) d'un groupe de travailleurs.
Lorsque les résultats des essais de confirmation dépassent l'AD, d'autres mesures devraient être effectuées afin de confirmer l'incorporation et une enquête devrait être réalisée pour déterminer la cause du résultat non prévu. Si l'incorporation est confirmée, les hypothèses relatives aux conditions d'exposition au rayonnement dans le lieu de travail et l'efficacité des mesures de protection en place doivent être examinées, et la nécessité pour les travailleurs concernés de participer à un programme d'essais biologiques devrait être réévaluée. Tous les résultats des essais de confirmation devraient être enregistrés.
Ce type de programme convient particulièrement bien aux radionucléides faciles à détecter à de faibles niveaux par rapport à l'AD.
Les essais de confirmation devraient être effectués pour vérifier les fondements d'un programme d'essais courants si des changements importants ont été apportés à l'installation ou aux opérations de l'installation. En outre, des essais de confirmation, à l'aide d'échantillonneurs d'air individuels ou de mesures d'essais biologiques individuels, devraient être effectués pour s'assurer que les résultats de la surveillance de l'air dans les lieux de travail peuvent être considérés comme étant représentatifs. [8]
3.0 Méthode et fréquence des essais biologiques
Il existe différentes méthodes d'échantillonnage pouvant être utilisées dans le cadre des essais biologiques (par exemple, l'analyse d'urine, le comptage du corps entier, le comptage thyroïdien), selon le type de matière radioactive manipulée et la fréquence de surveillance des travailleurs.
3.1 Méthodes d'essais biologiques
Les mesures effectuées dans le cadre des essais biologiques sont regroupées en deux catégories distinctes :
- les mesures d'essais biologiques in vivo : ce sont les mesures directes de la quantité de matières radioactives déposée dans les organes, les tissus ou le corps entier. Les méthodes courantes comprennent le comptage thyroïdien, le comptage pulmonaire et le comptage du corps entier.
- les mesures d'essais biologiques in vitro : ce sont les mesures de la quantité de matières radioactives contenues dans un échantillon provenant du corps humain. La méthode la plus courante est l'analyse d'urine. Il existe également d'autres méthodes, comme l'analyse des fèces, de l'haleine, et du sang.
Plusieurs facteurs devraient être considérés au moment de choisir la méthode d'essais biologiques. Le premier facteur est l'objectif de la surveillance—il devrait y avoir un équilibre entre les besoins liés à la surveillance de l'incorporation et l'évaluation de la dose [2]. La surveillance de l'incorporation exige des renseignements opportuns concernant les événements d'incorporation et devrait être basée sur les indicateurs d'incorporation suivants, par ordre de préférence :
- l'utilisation d'un échantillonneur d'air personnel (EAP) ou d'un échantillonneur d'air sur le lieu de travail (WPAS, de l'anglais workplace air sampler), où un échantillon d'air est prélevé dans l'espace d'air respirable du travailleur;
- le prélèvement nasal avec un coton-tige;
- les essais biologiques in vitro;
- les essais biologiques in vivo.
Les méthodes de contrôle de la dose sont, par ordre de préférence :
- les essais biologiques in vivo;
- les essais biologiques in vitro;
- l'utilisation d'un échantillonneur d'air personnel;
- l'échantillonnage de l'air sur le lieu de travail.
En plus de ces facteurs, les caractéristiques physiques des radionucléides en cause devraient être prises en compte. Certains radionucléides émettent un rayonnement ne pouvant être détecté depuis l'extérieur du corps. Dans ce cas, on peut mesurer un produit de désintégration, comme le 234Th, au moment d'évaluer la charge pulmonaire de 238U, en autant que les isotopes aient atteint l'équilibre séculaire. Ou encore, des essais biologiques in vitro peuvent être effectués. La méthode de mesure in vitro à privilégier dépend également de la rétention et de l'excrétion du radionucléide en question, y compris les voies prédominantes d'excrétion, par exemple la voie urinaire, les fèces et l'haleine.
Le tableau 2 montre les méthodes d'essais biologiques pouvant être effectuées pour divers radionucléides, compte tenu de leurs caractéristiques physiques et métaboliques. À noter que le tableau 2 n'est pas exhaustif et que le choix d'une méthode appropriée dépend de la forme physique et chimique du radionucléide, ainsi que de la voie d'excrétion.
Remarque : Dans les cas où la réalisation d'essais biologiques est inappropriée pour déterminer la dose, on peut utiliser plutôt des données de surveillance de l'air. Voir la section 3.2, Détermination de la fréquence.
Tableau 2 : Exemples de méthodes d'essais biologiques pour des radionucléides choisis
| Méthode d'essai biologique | Radionucléide | ||
|---|---|---|---|
| 1) In vivo | |||
| Comptage du corps entier | 51Cr 54Mn 59Fe 57Co, 58Co, 60Co 85Sr | 95Zr/95Nb 106Ru 110mAg 124Sb, 125Sb 134Cs, 137Cs | 144Ce 203Hg 226Ra, 228Ra 235U, 238U 252Cf |
| Comptage pulmonaire | 14C* 60Co 235U, 238U | 239Pu, 240Pu 241Am | 242Cm, 244Cm 252Cf |
| Comptage thyroïdien | 125I, 131I | ||
| 2) In vitro | |||
| Comptage à scintillateur liquide (comptage β) des échantillons d'urine | 3H 14C 32P, 33P | 35S 36Cl | 45Ca 129I |
| Comptage à scintillateur liquide des échantillons d'urine après séparation chimique | >14C | >89Sr ,90Sr | >228Ra |
| Comptage β du CO2 de l'haleine | 14C | ||
| Comptage β des échantillons fécaux après séparation chimique | 14C | ||
| Comptage β de l'eau tritiée dans l'haleine et la salive | 3H | ||
| Spectroscopie gamma des échantillons d'urine | 57Co, 58Co, 60Co | 85Sr 106Ru | 125I, 131I 134Cs, 137Cs |
| Spectroscopie gamma des échantillons fécaux (possiblement après séparation chimique) | 60Co | 144Ce | |
| Spectroscopie alpha des échantillons d'urine/de fèces après séparation radiochimique | 226Ra 228Th, 232Th 233U, 234U, 235U, 238U | 238Pu, 239Pu/240Pu** | 241Am 242Cm, 244Cm |
| Fluorimétrie, phosphorimétrie | Uranium | ||
| Spectrométrie de masse avec plasma à couplage inductif (en anglais, ICP-MS) | 234U, 235U, 236U, 238U | 238Pu, 239Pu | |
| SMIT | 239Pu, 240Pu | ||
* à l'aide d'un compteur de particules de type « scintillateur en sandwich » ou d'un compteur au germanium.
** La spectroscopie alpha ne permet pas habituellement de distinguer le 239Pu du 240Pu.
3.2 Détermination de la fréquence
Au moment de choisir la fréquence d'une surveillance courante, les principaux facteurs à prendre en compte sont les suivants :
- les caractéristiques du lieu de travail;
- l'incertitude liée au moment de l'incorporation;
- la sensibilité des instruments;
- la nécessité d'obtenir de l'information opportune sur les événements d'incorporation;
- le coût de la mise en œuvre du programme.
La forme physique et chimique de chaque radionucléide utilisé sur les lieux de travail doit être connue à la fois pour les conditions courantes et les conditions inhabituelles (ou encore pour les accidents). Ces formes déterminent le comportement biocinétique de chaque radionucléide et, par conséquent, les voies et les taux d'excrétion. En retour, ce comportement aide à déterminer la méthode d'essai biologique à employer.
La rétention et l'excrétion dépendent principalement de la forme chimique du radionucléide. Les composés inhalés sont classés dans trois catégories, selon le taux d'absorption entre les poumons et le sang : F (de l'anglais Fast, ou rapide), M (de l'anglais Moderate, ou modéré) et S (de l'anglais Slow, ou lent). Par exemple, un composé de type F, comme le UF6 est absorbé relativement rapidement dans le sang en provenance des poumons. Les composés de type S, comme le UO2, subsistent dans les poumons pendant une période de temps plus longue. Les valeurs des taux d'absorption par les poumons par défaut sont précisées dans la publication 66 de la CIPR (Commission internationale de protection radiologique), intitulée : Human Respiratory Tract Model for Radiological Protection, vol. 24, nos 1 à 3 [9] pour les trois types de clairance pulmonaire et pour les critères servant à la classification selon le type d'absorption, lorsque l'on utilise des données spécifiques au site pour caractériser l'air des lieux de travail.
Un autre facteur dont il faut tenir compte dans le choix de la fréquence de surveillance est l'incertitude liée à l'estimation de l'incorporation, en raison du fait que le moment de l'incorporation n'est pas connu (voir annexe B, Exemples, figures B3 et B4). En ce qui a trait à la surveillance hebdomadaire, il y a une incertitude importante associée au moment de l'incorporation dans le cas de l'excrétion urinaire (voir annexe B, figure B4), à cause des grands écarts dans le taux d'excrétion au cours des premiers jours suivant l'incorporation. Les résultats des mesures courantes devraient être évalués de manière à ce que l'incorporation soit considérée comme s'étant produite à mi-temps de la période de surveillance.
La sensibilité de l'instrument a une incidence importante sur la fréquence de la surveillance. Celle-ci doit être choisie de manière à s'assurer que les doses importantes ne sont pas manquées. Une dose peut être manquée lorsque, suite à une incorporation, la quantité dans le corps (qui dépend du taux d'excrétion) a été réduite à un niveau inférieur à la concentration mesurable minimale de l'instrument durant le temps qui s'est écoulé entre l'incorporation et la mesure. Lorsque cela est possible, la période de surveillance devrait être telle que les incorporations annuelles correspondant à une dose engagée totale de 1 mSv soient détectées. Si cela n'est pas réalisable, on doit avoir recours à la surveillance sur les lieux de travail et à l'échantillonnage de l'air personnel pour compléter la surveillance de l'incorporation. En appliquant le modèle métabolique approprié et en supposant un modèle d'incorporation, la période de surveillance adéquate peut être déterminée.
L'activité dérivée (AD) (mesurée en Bq ou en mg pour l'essai biologique in vivo, et en Bq/L ou en µg/L pour l'essai biologique in vitro) peut être définie comme suit :
![]()
où :
- T
- = la période de surveillance, en jours
- m(
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0) )
) - = la fraction de l'incorporation qui est retenue dans un tissu, un organe ou le corps entier, ou qui est excrétée par le corps, à mi-temps de la période de surveillance (voir annexe B, Exemples, figures B1 à B4); fonction du temps, dont les unités sont des « Bq par Bq incorporé », dans le cas des essais biologiques in vivo, et des Bq/L par Bq incorporé, dans le cas des essais biologiques in vitro
- LAI
- = Limite annuelle d'incorporation, en Bq/an
Les valeurs de m(![]() ) peuvent être consultées dans la publication 78 de la CIPR (Commission internationale de protection radiologique), intitulée : Individual Monitoring for Internal Exposure of Workers, Replacement of ICRP Publication 54 [7], portant sur la surveillance des incorporations de radionucléides.
) peuvent être consultées dans la publication 78 de la CIPR (Commission internationale de protection radiologique), intitulée : Individual Monitoring for Internal Exposure of Workers, Replacement of ICRP Publication 54 [7], portant sur la surveillance des incorporations de radionucléides.
La période maximale recommandée est celle où l'AD est égale à la concentration mesurable minimale. La limite de détection (c.-à-d. la concentration mesurable minimale) [10] peut être définie comme suit :
Concentration mesurable minimale = ![]()
où :
- K
- = un facteur d'étalonnage (K dépend du radionucléide et de l'efficacité de la détection), mesuré en (coups × L) / (secondes × Bq)
- t
- = le temps de comptage de la procédure, en jours
- σb
- = l'écart-type du nombre de coups obtenu pour le personnel non contaminé (nombre de coups « vides »)
Dans le cas des essais biologiques in vitro :
K = E V Y e-λΔt
où :
- E
- = l'efficacité du comptage, en (coups) / (secondes × Bq)
- V
- = la taille de l'échantillon en unités de masse ou de volume, en g ou L, selon le type d'échantillon
- Y
- = le rendement radiochimique fractionnaire, s'il y a lieu (pas d'unités) (Remarque : si non applicable, Y=1)
- λ
- = la constante de désintégration radioactive du radionucléide (1/secondes)
- Δt
- = le temps écoulé entre le prélèvement de l'échantillon et le comptage, en secondes
Dans le cas des essais biologiques in vivo, K est l'efficacité du comptage, y compris une correction pour l'auto-absorption, s'il y a lieu.
De façon générale, K doit être déterminé par le personnel qui effectue les mesures de l'essai biologique. On peut obtenir de plus amples renseignements sur les concentrations mesurables minimales dans l'American National Standard-Performance Criteria for Radiobioassay, Health Physics Society [10].
À l'aide de cette méthode servant à déterminer la période de surveillance, une période de surveillance recommandée d'un an serait peut-être possible pour certains radionucléides. Cependant, les taux de rétention et d'excrétion chez la plupart des personnes varient par rapport au modèle sur lequel les AD sont basées. En outre, de l'information opportune concernant les événements d'incorporation est requise. Il doit y avoir un équilibre entre l'utilisation des essais biologiques à titre d'indicateurs de l'incorporation et aux fins de l'évaluation de la dose. Pour tenir compte de cette situation, on pourrait choisir d'utiliser une période de surveillance plus courte qu'un an, selon les autres types de surveillance en place (comme la surveillance de l'air sur les lieux de travail), et selon le côté pratique de la réalisation des mesures d'essais biologiques. Des périodes de surveillance ont été recommandées dans les rapports portant sur des radionucléides spécifiques (comme l'évaluation de la dose imputable à l'uranium [11]). La norme ISO 20553 contient des propositions concernant la fréquence des essais pour différents radionucléides, ainsi que leur forme chimique typiques [8].
3.3 Autres considérations dosimétriques
En plus de la recommandation à l'effet que des incorporations de 1/20 de la LAI soient détectables pendant la durée de la période de surveillance, d'autres considérations dosimétriques peuvent être utilisées pour aider à déterminer la fréquence des essais biologiques.
Dans la publication 54 de la CIPR, intitulée Individual Monitoring for Intakes of Radionuclides by Workers: Design and Interpretation [12], la CIPR recommande que la précision des mesures soit supérieure à un facteur de 2 pour l'intervalle de confiance de 95 %, dans le cas des doses reçues en provenance de sources d'exposition externes, mais en ce qui a trait aux expositions internes, ce niveau de précision n'est pas toujours possible. Les incertitudes dues au fait que le moment de l'incorporation n'est pas connu n'est qu'une des composantes de l'incertitude globale associée au calcul de la dose. Les périodes de surveillance recommandées dans la publication 78 de la CIPR, intitulée : Individual Monitoring for Internal Exposure of Workers, Replacement of ICRP Publication 54 [7], accepte un facteur de 3 pour ce qui est de l'incertitude due au fait que le moment de l'exposition n'est pas connu pendant la période de surveillance. S'il y a plusieurs périodes de surveillance durant l'année, l'incertitude globale associée à l'incorporation annuelle, ainsi que la dose engagée seront probablement inférieures à ce facteur de 3 [7]. L'exposition à certaines sources internes, comme les faibles concentrations d'eau tritiée dans certains milieux de réacteurs CANDU, peut se produire de façon continue pendant la période de surveillance.
Dans certains cas, les meilleures méthodes de surveillance disponibles ne permettront pas de détecter de manière fiable des activités correspondant à 1/20 LAI (1 mSv par année). Dans ces circonstances, il est utile de déterminer la dose maximale qui pourrait être manquée si l'incorporation se produit au début de chaque période de surveillance. Une telle méthode fournit une perspective utile pour certains dangers internes qui sont difficiles à détecter [13], mais peuvent devenir inutilement conservatrices, particulièrement lorsqu'on dénombre plusieurs périodes de surveillance par année.
4.0 Interprétation des résultats
4.1 Niveaux de référence
Un niveau de référence est une valeur de paramètres mesurée au-delà de laquelle des actions spécifiées ou des décisions devraient être prises, afin d'éviter la perte de contrôle d'une partie du programme de radioprotection (PRP) du titulaire de permis. Habituellement, le niveau de référence est inférieur au seuil d'intervention indiqué dans le PRP.
Des niveaux de référence peuvent être utilisés pour interpréter les données de surveillance sur les lieux de travail ou les données de surveillance associées aux essais biologiques et pour signaler les incorporations potentielles. Ces niveaux, qui sont applicables aux programmes courants ou spéciaux de surveillance relatifs aux essais biologiques, permettent une réponse progressive aux incorporations potentielles et, par conséquent, ne constituent pas une limite réglementaire en soi. Les niveaux de référence sont habituellement exprimés sous la forme de fractions de la LAI. La somme des ratios (incorporation par rapport à la LAI) devrait être utilisée lorsque plus d'un radionucléides sont en cause.
Étant donné que les programmes d'essais biologiques permettent rarement de mesurer l'incorporation, les niveaux de référence dérivés–exprimés en termes de quantité mesurée–sont généralement une quantité plus utile. Le niveau de référence dérivé est l'activité déterminée par l'essai biologique, attribuable aux sources en milieu de travail. Le niveaux de référence dérivé pour une mesure d'essai biologique en particulier, est exprimée dans les mêmes unités que les résultats de mesure de l'essai biologique. Dans le cas des programmes d'essais biologiques courants, les niveaux de référence devraient être basés sur l'hypothèse d'une incorporation à mi-temps de la période de surveillance.
Pour certains radionucléides et certains types d'essais biologiques, les sources attribuables à des sources autres que les sources en milieu de travail peuvent faire en sorte que les résultats courants dépassent le niveau de la décision analytique et un niveau de référence dérivé. Si les résultats de l'essai biologique dépassent régulièrement ou souvent un niveau de référence dérivé due à des sources autres que les sources en milieu de travail, le niveau de référence dérivé peut être augmenté si les résultats prévus de l'essai biologique, dus à de telles sources, sont connus (une étude utilisant un groupe témoin ayant reçu une exposition non professionnelle semblable, mais sans risque d'exposition professsionnelle, peut être utilisée à cette fin). Le niveau de référence dérivé ainsi ajusté est fixé à une valeur ne dépassant pas le 99e percentile du groupe témoin [2]. Si les niveaux non professionnels dépassent le niveau d'enquête dérivé (NED), d'autres méthodes de surveillance de l'incorporation devraient être utilisées si possible.
Les niveaux de référence utilisés dans ce rapport sont l'AD, le niveau d'enquête (NE), et le niveau d'enquête dérivé (NED). L'AD est définie à la section 3.2, Détermination de la fréquence. Le NE et le NED sont définis ci-après.
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0)
![]()
où :
- T
- = la période de surveillance, en jours
- m(
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0) )
) - = la fraction de l'incorporation qui est retenue dans un tissu, un organe, ou le corps entier, ou qui est excrétée du corps, à mi-temps de la période de surveillance; une fonction du temps, dont les unités sont des « Bq par Bq d'incorporation », dans le cas des essais biologiques in vivo, et des Bq/L par Bq d'incorporation, dans le cas des essais biologiques in vitro
Un tableau illustrant des exemples de NED pour l'inhalation de composés de 137Cs de type F est donné à l'annexe B, Exemples, tableau B2.
Afin de tenir compte de la limite de dose réduite reçue par les travailleuses enceintes, un NED devrait être fixé pour celles-ci. La durée de la grossesse est habituellement de 37 à 42 semaines (entre 9 et 10 mois), et la limite de dose pour la travailleuse enceinte est de 4 mSv pour le reste de la grossesse (c'est-à-dire à partir du moment où la travailleuse informe le titulaire de permis). Selon des hypothèses prudentes (par exemple, lorsque la grossesse est déclarée immédiatement), veiller à ce que la dose reçue par la travailleuse enceinte ne dépassse pas 0,4 mSv par mois aidera à assurer que la limite de 4 mSv ne soit pas dépassée. Par conséquent, un NED pour les travailleuses enceintes, le NEDTE, peut être défini comme suit :
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0)
4.2 Mise en perspective des résultats des essais biologiques
Les résultats des essais biologiques peuvent être interprétés en les comparant avec les niveaux de référence dérivés. Le tableau 3 fournit les niveaux de référence suggérés qui peuvent servir de fondement à l'interprétation des résultats d'essais biologiques et dicter les mesures appropriées à prendre.
Tableau 3 : Niveaux de référence dérivés et réponses correspondantes recommandées
| Résultat d'essai biologique | Réponse recommandée |
|---|---|
| < AD | Enregistrer le résultat de la mesure de l'essai biologique. |
| AD ≤ résultat < NED | Confirmer et enregistrer le résultat de la mesure de l'essai biologique. Si le résultat est confirmé, évaluer la DEE. |
| ≥ NED | Confirmer et enregistrer le résultat de la mesure de l'essai biologique. Si le résultat est confirmé, évaluer la DEE. Enquêter pour trouver et corriger la cause de l'incorporation. |
Pour évaluer la DEE, les résultats de l'essai biologique doivent d'abord être combinés avec m(T/2) pour estimer l'incorporation :
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0)
La DEE peut être estimée à l'aide de la formule suivante :
DEE = Incorporation × e(50)
où e(50) (mesurée en Sv/Bq) est la dose par incorporation unitaire pour le radionucléide, la taille de particules et la forme chimique en cause [14]. Si plus de 10 % environ de la quantité réelle mesurée peut être attribuée à des incorporations associées aux intervalles précédents, pour lesquels l'incorporation et la dose ont déjà été évaluées, des corrections devraient être apportées [7].
4.3 Précision des résultats d'essais biologiques
De nombreux composants contribuent à la précision globale de l'estimation de la dose. Ceux-ci comprennent la précision :
- du système de détection;
- de la méthode de mesure;
- du modèle biologique utilisé pour établir un lien entre la radioactivité interne observable et la dose de rayonnement reçue;
- de l'incertitude du temps réel d'internalisation de la radioactivité par rapport au moment de la mesure de l'essai biologique.
La présente section ne porte que sur la précision des composants 1 et 2. Tous les aspects de l'incertitude du modèle biologique, qui peuvent parfois être la source prédominante des inexactitudes et des incertitudes dans l'estimation de la dose finale, sont examinés dans le document Reliability of the ICRP's Systemic Biokinetic Models, Radiation Protection Dosimetry, Vol. 79, R.W. Leggett [15]. Les incertitudes associées au moment de l'incorporation par rapport au moment auquel la surveillance est effectuée sont examinées brièvement à la section 3.2, Détermination de la fréquence.
Lors de la conception et de l'établissement d'un programme d'essais biologiques, il est important de tenir compte de la précision des instruments en rapport avec la mesure à prendre. Le système complet de mesure devrait être tel que toute erreur dans la mesure finale n'aura qu'une incidence mineure sur la précision globale de la dose de rayonnement estimée reçue par le travailleur. Comme certaines incertitudes sont importantes (par exemple les points 3 et 4), on estime qu'il est acceptable que l'incertitude de la composante « instrument de détection » soit à l'intérieur d'une plage de -25 % à +50 % [16].
Les considérations suivantes devraient être incluses dans l'évaluation de la précision des instruments de détection et de la méthode de mesure :
- L'erreur de comptage statistique nette.
Cela comprend l'erreur statistique dans le comptage de l'essai biologique et l'erreur statistique dans la mesure du taux de comptage du rayonnement de fond. Le taux de comptage du rayonnement de fond doit être approprié à la norme, à l'échantillon ou au sujet. - L'erreur causée par des variations dans la géométrie de comptage.
Cela doit comprendre les tolérances relatives aux écarts physiques chez les sujets ou dans les échantillons ayant fait l'objet d'un comptage, particulièrement en ce qui a trait à l'équipement de comptage spécifique utilisé. - L'erreur introduite par l'atténuation du rayonnement émis par les tissus sus-jacents durant le comptage in vivo.
L'effet des tissus sus-jacents devrait être considéré lorsque l'émission gamma du nucléide en question est inférieure à 200 keV [7], ou lorsque le rayonnement de freinage (Bremsstrahlung) associé aux émissions bêta sont comptés. Ceci nécessite une évaluation de la profondeur et de la densité moyennes des tissus sus-jacents, qui peuvent varier considérablement d'une personne à une autre. - L'étalonnage de l'instrument en fonction de l'isotope mesuré dans une géométrie pertinente pour la mesure réelle.
L'instrument employé pour l'essai biologique devrait être étalonné en fonction de l'isotope en cause et un programme de contrôle de la qualité régulier devrait être en place, afin de s'assurer que l'étalonnage est effectué sur une base régulière. Des vérifications internes fréquentes à l'aide d'une source radioactive à longue période doivent également être effectuées sur une base régulière, pour confirmer que la réponse du détecteur est constante au fil du temps et qu'il fonctionne correctement [16].
L'exemple 2 de l'annexe B, Exemples, contient un exemple de calcul de l'erreur de comptage pour un résultat d'essai biologique.
5.0 Enregistrement des résultats d'essais biologiques
Un registre d'essais biologiques permet de retracer les données de dose en vue de reconstituer éventuellement la dose.
Afin de se conformer à l'article 27 de la LSRN, la Section 28 du Règlement général sur la sûreté et la réglementation nucléaires et le paragraphe 5(1) et l'article 24 du Règlement sur la radioprotection, un registre d'essais biologiques doit être tenu pour chaque personne qui participe au programme d'essais biologiques. De plus, ce registre doit clairement identifier l'employé par son nom ainsi que son groupe de travaille. Plus de renseignements pourraient être exigés afin de se conformer avec toute condition de permis pertinente. Pour chaque période de dosimétrie, les données relatives aux essais biologiques devraient être conservées, ainsi que la date à laquelle la mesure a été prise. Les registres devraient également comprendre un contrôle de la qualité des instruments, les résultats de l'étalonnage et les registres de traçabilité avec des laboratoires primaires et secondaires. [16]
Annexe A : Choix des participants à un programme d'essais biologiques courants basé sur l'activité manipulée
L'orientation sur le choix des participants à un programme d'essai biologique courant basé sur l'activité manipulée ou sur l'activité associée à des procédés est fournie dans diverses références [2, 5, 17]. Les valeurs indiquées au tableau 1 ont été principalement basées sur la méthode présentée dans le document American National Standard-Design of Internal Dosimetry Programs, Health Physics Society; toutefois, des valeurs semblables peuvent être obtenues dans d'autres références.
Fraction d'incorporation potentielle (FIP)
La fraction d'incorporation potentielle (FIP) est définie comme suit :
FIP = 10-6 × R × C × D × O × S
où :
- 10-6
- = facteur de Brodsky [18]
- R
- = facteur de rejet
- C
- = facteur de confinement
- D
- = facteur de dispersabilité
- O
- = facteur d'occupation des locaux
- S
- = facteur relatif aux matières sous forme spéciale
Facteur de rejet (R)
| Gaz, liquides fortement volatils | 1,0 |
| Poudres non volatiles, liquides légèrement volatils | 0,1 |
| Liquides, contamination d'une vaste étendue | 0,01 |
| Solides, contamination ponctuelle, matières contenues dans des particules de grande taille; par exemple, résines | 0,001 |
| Matières encapsulées | 0 |
Facteur de confinement (C)
| Boîte à gants ou cellule chaude | 0,01 |
| Hotte améliorée (enceinte fermée, avec ouvertures pour les bras) | 0,1 |
| Hotte | 1,0 |
| Matières contaminées contenues dans des sacs, ou enveloppées, matières contenues dans des sacs et placées dans des boîtes de bois ou de carton, serres | 10 |
| Table de travail, contamination de surface dans une salle où la ventilation est normale | 100 |
Facteur de dispersabilité (D)
| Mesures qui accroissent l'énergie des matières (chauffage, coupe, meulage, usinage, soudage, mise sous pression, réactions exothermiques) | 10 |
| Autres mesures (qui ne favorisent pas la dispersabilité) | 1 |
Facteur d'occupation des locaux (O)
| Utilisation annuelle ou unique | 1 |
| Utilisation mensuelle ou à quelques reprises durant l'année | 10 |
| Utilisation hebdomadaire, une dizaine de fois durant l'année, ou des dizaines de jours lors d'un projet ponctuel | 50 |
| Utilisation quotidienne essentiellement | 250 |
Facteur relatif aux matières sous forme spéciale (S)
| Précurseurs de l'ADN (sauf 32P, 35S, ou 131I) | 10 |
| Autres matières | 1 |
Valeurs du tableau 1
| Gaz et liquides volatils | R = 1 (gaz, liquides fortement volatils) D = 1 (aucune énergie communiquée au système) O = 250 (utilisation quotidienne essentiellement) S = 1 |
| Poudres | R = 0.1 D = 1 (aucune énergie communiquée au système) O = 250 (utilisation quotidienne essentiellement) S = 1 |
| Liquides et solides non volatils | R = 0,01 (liquids, large area contamination) D = 1 (aucune énergie communiquée au système) O = 250 (utilisation quotidienne essentiellement) S = 1 |
Annexe B : Exemples
B.1 Exemple 1 : Détermination de la participation à un programme d'essais biologiques
Un travailleur manipule en moyenne :
- 1 × 106 Bq de 125I, trois fois par semaine, sous une hotte (en supposant que l'ingestion est la voie d'incorporation la plus probable);
- 1 × 107 Bq de 3H (sous forme d'eau tritiée), presque quotidiennement, sous une hotte (en supposant qu'il y a ingestion);
- 0,6 × 106 Bq de 131I, quatre fois par année, sur une table de travail (en supposant qu'il y a inhalation).
Toutes les matières radioactives se présentent sous une forme relativement volatile.
Les paramètres suivants doivent être déterminés :
- l'incorporation totale par année;
- le coefficient de conversion de dose (cet exemple utilise un coefficient de conversion de dose de e(50), selon la publication 68 de la CIPR [14]);
- la limite annuelle d'incorporation (LAI);
- la fraction d'incorporation potentielle (FIP) - (voir annexe A)
- les coefficients rj, où j = A, B, et C (correspondant aux trois incorporations de radionucléides définies ci-dessus);
- la somme des coefficients Rj, où Rj =rA + rB + rC.
Le tableau B1 montre des exemples de calcul étape par étape, dans le but de déterminer les valeurs de rj et de Rj.
Dans le cas qui nous occupe, les résultats des calculs figurant au tableau B1 sont :
- Rj < 1, par conséquent (et conformément à la section 4.2, Mise en perspective des résultats des essais biologiques), le travailleur n'est pas obligé de faire l'objet d'une surveillance relative à des essais biologiques.
- Cependant, rA = 0,38 > 0,3, alors le titulaire de permis peut choisir d'effectuer un contrôle du rayonnement pour le travailleur afin de détecter le 125I.
Tableau B1 : Évaluation des coefficients rj et du coefficient de somme Rj
| 125I (ingestion) | 3H (ingestion) | 131I (inhalation) | |
|---|---|---|---|
| Incorporation | 1 MBq par séance | 10 MBq par séance | 0,6 MBq par séance |
| Incorporation totale par année | 106 × (3 × 52) = 0,16 GBq/year | 107 × (5 × 52) = 2,6 GBq/year | 0,6 × 106 × 4 = 2,4 MBq/year |
| Coefficient de conversion de dose e(50) (se reporter à la publication 68 de la CIPR) | 1,5 × 10-8 Sv/Bq | 1,8 × 10-11 Sv/Bq | 2,0 × 10-8 Sv/Bq |
Limite annuelle d'incorporation (LAI), où :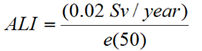 | 1,3 MBq/année | 1,1 GBq/année | 1,0 MBq/année |
| Fraction d'incorporation potentielle (FIP) (voir annexe A) | Facteur d'occupation des locaux = 3 × 52 | Occupancy factor = 250 Facteur de confinement = 1 FIP = 2,5 × 10-4 | Facteur d'occupation des locaux = 4 Facteur de confinement = 100 FIP = 4 × 10-4 |
Ratios rj, où :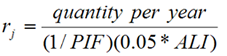 | 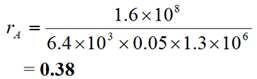 | 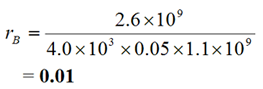 | 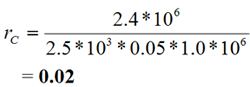 |
| Somme des ratios, rj | |||
B.2 Exemple 2 : Détermination de l'erreur de comptage (incertitude)
Les étapes à suivre pour calculer l'erreur associée au système de détection (statistique de comptage), ainsi qu'une démonstration du calcul de l'erreur de comptage à partir d'un résultat unique d'essai biologique sont illustrées ci-après :
(a) Résultats d'une mesure directe :
- Comptage de l'échantillon :
- 25 077 (par litre d'urine)
- Temps de comptage de l'échantillon :
- 10 minutes
- Comptage du rayonnement de fond :
- 4 300 (par litre d'urine)
- Temps de comptage du rayonnement de fond :
- 20 minutes
À la lumière de ces données, les taux de comptage sont calculés comme suit :
- Taux de comptage de l'échantillon
- = (comptage de l'échantillon) / (temps de comptage de l'échantillon)
= 25 077/10 min
= 2 508 coups par minute (cpm)
De même, le taux de comptage du rayonnement de fond est calculé comme suit :
- Taux de comptage du rayonnement de fond
- = (comptage du rayonnement de fond) / (temps de comptage du rayonnement
de fond)
= 4 300/20 min
= 215 cpm
(b) Taux de comptage net :
Le taux de comptage du rayonnement de fond est soustrait du taux de comptage de l'échantillon afin d'obtenir le taux de comptage net :
2 508 – 215 = 2 293 cpm
(c) Estimation de l'erreur de comptage : [19]
L'erreur de comptage (pour l'intervalle de confiance de 95 % basé seulement sur les statistiques de comptage) est donc calculée comme suit :

Ainsi, le taux de comptage de l'échantillon est de 2 293 ± 32 cpm. L'erreur statistique de 32 cpm représente l'erreur relative de (32 cpm) / (2 293 cpm) = 1,4 %.
(d) Résultat des mesures et de l'analyse :
Si l'efficacité du détecteur pour le 137Cs est de 10 %, le nombre de désintégrations par minute (dpm) est donné par :
(taux de comptage net) / (efficacité) = 2 293/0,10 = 22 930 dpm
Pour exprimer ce résultat en désintégrations par seconde, ou en becquerels (Bq), il suffit de diviser par 60, et nous obtenons 382 Bq. L'erreur relative de 1,4 % est reportée dans l'équation suivante :
382 Bq × 1,4 % = 5 Bq
Le résultat obtenu pour l'échantillon de l'essai biologique, incluant l'erreur statistique seulement, est donc donné par :
(382 ± 5 Bq/L) × (1,6 L/jour) = 611 ± 8 Bq/jour, en supposant une élimination d'urine de 1,6 L quotidiennement pour l'homme de référence [20]
(e) Conclusion
Dans cet exemple, nous avons tenu compte seulement d'une incertitude, soit la statistique de comptage. D'autres facteurs, comme la géométrie du comptage ou les erreurs d'étalonnage, peuvent accroître l'incertitude.
B.3 Exemple 3 : Détermination de la fréquence de surveillance des incorporations de 137Cs
Le tableau 2 de la section 3.1, Méthodes d'essais biologiques, montre que le comptage du corps entier et l'analyse d'urine (comptage gamma) sont des méthodes appropriées pour détecter le 137Cs. La période de surveillance pour le comptage du corps entier est examinée en premier lieu.
L'activité dérivée (AD) est l'activité mesurable qui indique une dose de 1 mSv ou plus par rapport à la dose efficace engagée. La valeur seuil doit être déterminée de manière fiable, c'est-à-dire que l'AD doit être supérieure à la concentration mesurable minimale (CMM). Si elle est inférieure à la CMM, la concentration mesurée devient non pertinente. L'AD dépend du temps qui s'écoule entre les mesures de surveillance (période de surveillance). Dans le présent exemple, le cas d'une incorporation par inhalation de 137Cs est étudié.
Essai biologique in vivo :
La figure B1 illustre l'AD en fonction de la période de surveillance. La limite de détection (CMM) a été superposée au graphique. Cette figure montre que l'AD demeure au-dessus de la CMM pour un large éventail de période de surveillance. Toute période, allant jusqu'à un an, pourrait donc constituer un intervalle raisonnable entre les essais biologiques à des fins de surveillance. Pour déterminer la période optimale de surveillance, d'autres considérations décrites à la Section 3.2, Détermination de la fréquence, doivent être prises en compte.
Figure B1 : Inhalation aiguë de 137Cs de type F; essai biologique (corps entier). L'activité dérivée est représentée en fonction de la période de surveillance (temps qui s'écoule entre les mesures)
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0)
Essai biologique in vitro :
La figure B2 représente l'AD en fonction des périodes de surveillance. La courbe est obtenue en appliquant les définitions de la Section 3.2, Détermination de la fréquence. L'AD est comparée à la CMM. La courbe de l'AD demeure bien au-dessus de la ligne horizontale qui représente la CMM à 1 Bq/L pendant la période présentée au tableau [7] allant de 7 jours à un an. Le choix d'une période de surveillance spécifique comprend d'autres facteurs, décrits à la Section 3.2.
Figure B2 : Inhalation aiguë de 137Cs de type F, essai biologique in vitro (excrétion urinaire). L'activité dérivée est représentée en fonction de la période de surveillance (temps qui s'écoule entre les mesures).
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0)
B.4 Exemple 4 : Détermination de la fréquence de surveillance des incorporations de 131I
Une concentration mesurable minimale atteignable de 100 Bq pour la surveillance thyroïdienne visant à détecter le 131I a été proposée [7]. Comme dans l'exemple précédent, l'AD est représentée graphiquement en fonction de différentes périodes de surveillance, allant de 2 à 180 jours. Le résultat est illustré à la figure B3.
D'après le graphique, il est clair que si la période de surveillance est inférieure à quatre (4) jours, ou supérieure à 65 jours, l'activité du 131I dans la thyroïde est inférieure à la concentration mesurable minimale et que, pour cette raison, elle n'est pas détectée. Dans ce cas, une période de 14 ou 30 jours constituerait un intervalle optimal entre les essais.
Figure B3 : 131I dans la thyroïde (inhalation aiguë de vapeur) – Activité dérivée en fonction du temps
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0)
Bien que le 131I puisse être détecté grâce aux mesures in vitro, la figure B4 laisse supposer qu'après cinq (5) jours, la quantité de 131I excrétée est inférieure à la concentration mesurable minimale de 1 Bq/L [7]. En outre, le taux d'excrétion de l'iode radioactif varie d'une personne à une autre et dépend de plusieurs facteurs, y compris la diète, l'âge et la prise de médicaments. Les écarts dans le taux d'excrétion entre les individus peut être important et, par conséquent, une période de surveillance de cinq (5) jours ne permet pas toujours de détecter 1 AD. Dans ce cas, l'analyse d'urine n'est pas recommandée à titre de méthode de surveillance courante pour évaluer les incorporations de 131I.
Figure B4 : Activité dérivée pour l'excrétion urinaire du 131I suite à une inhalation aiguë de vapeur
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0)
B.5 Exemple 5 : Niveaux d'enquête dérivés pour l'inhalation de 137Cs
Les niveaux d'enquête dérivés (NED) pour l'activité dans le corps entier et l'excrétion urinaire, en cas d'inhalation 137Cs de type F, sont calculés à l'aide des valeurs de m(T/2) tirées de la publication 78 de la CIPR (Commission internationale de protection radiologique), intitulée : Individual Monitoring for Internal Exposure of Workers, Replacement of ICRP Publication 54 [7]. Pour ce qui concerne la rétention dans le corps entier, sur une période de surveillance courante de 14 jours, les paramètres sont les suivants :
- Période de surveillance :
- T = 14 jours
- Rétention dans le corps entier à T/2 :
- m(7 jours) = 0,42
- LAI
- = 3 × 106 Bq[14]
.png/object?subscription-key=3ff0910c6c54489abc34bc5b7d773be0)
Les valeurs du NED pour le corps entier et pour l'excrétion urinaire, dans le cas des périodes de surveillance courante de 14 à 180 jours, sont illustrées au tableau B2. Les valeurs s'appliquent à l'inhalation du 137Cs de type F.
Tableau B2 : Niveaux d'enquête dérivés (NED) pour la surveillance courante du 137Cs
| Intervalle de surveillance | NED : Activité dans le corps entier | NED : Excrétion urinaire quotidienne (Bq/jour) | NED : Excrétion urinaire |
|---|---|---|---|
| 14 | 1,4 × 104 | 1,3 × 102 | 9,1 × 101 |
| 30 | 2,9 × 104 | 1,6 × 102 | 1,1 × 102 |
| 60 | 5,4 × 104 | 2,7 × 102 | 1,9 × 102 |
| 90 | 7,3 × 104 | 3,7 × 102 | 2,6 × 102 |
| 180 | 1,1 × 105 | 5,5 × 102 | 3,9 × 102 |
Glossaire
- Activité dérivée (AD)
- La rétention ou le taux d'excrétion attendue, exprimé soit en Bq ou en Bq/jour, résultant d'une mesure unique d'un radionucléide, obtenue à la fin d'une période de surveillance qui est tel que la dose efficace engagée annuelle correspondante extrapolée est égale à 1 mSv. L'AD est calculée en supposant que l'incorporation ait eu lieue au point milieu de la période de surveillance.
- Concentration mesurable minimale
- Quantité la plus faible (activité ou masse) d'un radionucléide (ou d'une substance à analyser) dans un échantillon, qui sera détectée avec une probabilité de non-détection (erreur de type II), tout en ayant une probabilité de conclure fautivement qu'une quantité positive (différente de zéro) de la substance à analyser est présente dans un « échantillon à blanc » approprié (erreur de type I) ; mesurée en Bq/L.
- Dose absorbée (D)
- L'énergie absorbée lors d'une exposition au rayonnement par masse unitaire. L'unité SI de la dose absorbée est le gray (Gy).
- Dose efficace (E)
- Somme, exprimée en sieverts, des valeurs dont chacune représente le produit de la dose équivalente reçue par un organe ou un tissu, et engagée à leur égard, figurant à la colonne 1 de l'annexe 1 (Règlement sur la radioprotection) par le facteur de pondération du tissu figurant à la colonne 2 (Règlement sur la radioprotection).
- Dose efficace engagée (DEE) (E(50))
- La dose efficace résultant de l'incorporation d'une substance radioactive. Cette dose est accumulée sur une période de 50 ans suivant l'incorporation initiale. L'unité SI de la DEE est le sievert (Sv).
- Dose équivalente (HT)
- Produit, exprimé en sieverts, de la dose absorbée d'un type de rayonnement figurant à la colonne 1 de l'annexe 2 (Règlement sur la radioprotection) par le facteur de pondération du rayonnement figurant à la colonne 2 (Règlement sur la radioprotection).
- Échantillonneur d'air sur le lieu de travail (WPAS)
- Échantillonneur d'air WPAS (de l'anglais Workplace Air Sampler) constitué d'un porte-filtre et d'une pompe à vide, qui est installé dans une zone de travail dans le but d'estimer les concentrations de radionucléides dans l'air respirable qui l'entoure.
- Échantillonneur d'air personnel (EAP)
- Échantillonneur d'air constitué d'un porte-filtre et d'une pompe à vide à piles, et qui est porté par le travailleur dans le but d'estimer les concentrations de radionucléides dans l'air respirable qui l'entoure.
- Essai biologique
- Mesure de la quantité ou de la concentration d'un radionucléide dans le corps ou dans une matière biologique excrétée ou retirée du corps et analysée dans le but d'estimer la quantité de radionucléide dans le corps.
- Essai biologique in vitro
- Mesures visant à détecter la présence de matières radioactives, ou à en estimer la quantité dans les fèces ou dans d'autres matières biologiques excrétées ou retirées du corps.
- Essai biologique in vivo
- Mesures d'une matière radioactive présente dans le corps à l'aide d'instruments qui détectent le rayonnement émis par cette matière, à l'intérieur du corps.
- Facteur de pondération des tissus
- Facteur pour lequel la dose équivalente est pondérée aux fins de la détermination de la dose efficace. Le facteur de pondération des tissus pour un organe ou un tissu représente la contribution relative de cet organe ou de ce tissu au préjudice total causé par les effets de l'irradiation uniforme du corps entier [21].
- Facteur de pondération du rayonnement
- Facteur pour lequel la dose absorbée est pondérée dans le but de déterminer la dose équivalente. Le facteur de pondération du rayonnement pour un type spécifique et une énergie de rayonnement a été choisi afin d'être représentatif de l'efficacité biologique relative (EBR) de ce rayonnement en ce qui a trait à la production d'effets stochastiques à de faibles doses. L'EBR d'un rayonnement, comparativement à un autre, est le rapport inverse des doses absorbées produisant le même degré d'un point final biologique défini [21].
- Fonction d'excrétion (m)
- Expression mathématique de la fraction d'excrétion d'un radionucléide hors du corps à n'importe quel moment suite à l'incorporation, généralement exprimée en becquerels excrétés par jour, par becquerel incorporé.
- Fraction d'incorporation potentielle (FIP)
- Quantité sans dimension qui définit l'incorporation comme étant une fraction de l'exposition à la contamination. La fraction d'incorporation dépend de plusieurs facteurs : rejet, confinement, dispersabilité, facteur d'occupation. Par exemple, FIP=0 dans le cas des matières encapsulées, étant donné qu'il n'y a, dans ce cas, aucune incorporation de substances nucléaires radioactives dans le corps d'un travailleur.
- Incorporation
- Quantité d'un radionucléide, mesurée en Bq, qui a été incorporée par inhalation, absorption cutanée, injection, ingestion, ou par le biais de blessures.
- Limite annuelle d'incorporation (LAI)
- L'activité d'un radionucléide qui, lorsqu'il est incorporé, résulte en une DEE de 20 mSv.
- Limite dérivée de concentration dans l'air (LDCA)
- Concentration d'un radionucléide dans l'air qui, lorsqu'il est inhalé à un rythme respiratoire de 1,5 m3 par heure, pendant 2 000 heures dans une année, résulte en une incorporation de 1 LAI.
- Modèle de biocinétique
- Description mathématique du comportement des radionucléides dans les réactions métaboliques qui se produisent dans les cellules, les tissus, les organes et les organismes. On utilise surtout ce modèle pour décrire la répartition des radionucléides dans les tissus et leur excrétion.
- Niveau de décision analytique (niveau critique)
- Mesure du nombre de coups enregistrés par un instrument, ou mesure finale de l'instrument effectuée pour détecter une quantité d'une substance à analyser, pour laquelle ou au-delà de laquelle une décision est prise à l'effet qu'une quantité positive de cette substance est présente; mesurée en Bq/L.
- Niveau d'enquête (NE)
- Indicateur de l'incorporation (en Bq) de substances radioactives qui nécessite une surveillance spéciale du travailleur. Cet indicateur est habituellement exprimé comme étant une fraction de la LAI.
- Niveau d'enquête dérivé (NED)
- Lorsqu'un programme de surveillance de la contamination interne est en place, il convient de déterminer, à l'avance, les niveaux de contamination au-delà desquels certaines mesures sont requises. Le niveau d'enquête dérivé (NED) est le niveau auquel une enquête ou une évaluation de la dose est initiée, mesurée en Bq.
- Niveau de référence dérivé
- Activité déterminée par l'essai biologique, attribuable aux sources en milieu de travail, mesurée en Bq/L.
- Période biologique
- Temps nécessaire pour qu'un organisme, tel qu'un organisme humain, élimine par les voies naturelles (autres que la désintégration radioactive) la moitié d'une quantité de radionucléides incorporée.
- Rayonnement de freinage (Bremsstrahlung)
- Rayonnement électromagnétique produit par la décélération d'une particule chargée, comme un électron, lorsque celle-ci est déviée (changement de la quantité de mouvement) par une autre particule chargée, comme le noyau d'un atome.
- Sievert (Sv)
- Unité de dose équivalente, de dose efficace et de DEE. Un sievert est défini comme étant un joule d'énergie absorbée par kilogramme de tissu, multiplié par un facteur de pondération approprié, sans dimension. Voir également « dose équivalente » et « dose efficace ».
- Travailleur du secteur nucléaire (TSN)
- Personne qui, du fait de sa profession ou de son occupation et des conditions dans lesquelles elle exerce ses activités, si celles-ci sont liées à une substance ou une installation nucléaire, risque vraisemblablement de recevoir une dose de rayonnement supérieure à la limite réglementaire fixée pour la population en général.
Références
- U.S. Department of Energy, DOE Standard Internal Dosimetry, DOE-Std-1121-98, 1999.
- Health Physics Society, American National Standard-Design of Internal Dosimetry Programs, ANSI/HPS N13.39-2001.
- Commission canadienne de sûreté nucléaire (CCSN), Contrôle et enregistrement des doses de rayonnement aux personnes, Guide d'application de la réglementation G-91, 2003(a).
- CCSN, Conception et mise en œuvre d'un programme d'essais biologiques, Rapport du groupe de travail de la CCSN sur la dosimétrie interne, RSP-0182A.
- Agence internationale de l'énergie atomique, Évaluation de l'exposition professionnelle due à l'incorporation de radionucléides, Guide de sûreté no RS-G-1.2, 1999.
- CCSN, Protocoles d'intervention pour les essais biologiques en cas d'incorporation anormale de radionucléides, Guide d'application de la réglementation G-147, 2003(b).
- Commission internationale de protection radiologique (CIPR), Individual Monitoring for Internal Exposure of Workers, Replacement of ICRP Publication 54, Publication 78, Pergamon Press, 1997.
- ISO 20553:2006, Radioprotection—Surveillance professionnelle des travailleurs exposés à un risque de contamination interne par des matériaux radioactifs.
- CIPR, Human Respiratory Tract Model for Radiological Protection, Publication 66, Vol. 24, nos 1 à 3, Pergamon Press, 1994.
- Health Physics Society, American National Standard-Performance Criteria for Radiobioassay, HPS N13.30-1996.
- CCSN, Uranium Intake-Dose Estimation Methods, Rapport du Groupe de travail sur la dosimétrie interne de la CCSN, RSP-0165, 2003(c).
- CIPR, Individual Monitoring for Intakes of Radionuclides by Workers: Design and Interpretation, Publication 54, 1989.
- Santé et Bien-être social Canada, Bioassay Guideline 4—Guidelines for Uranium Bioassay, 88-EHD-139, 1987.
- CIPR, Dose Coefficients for Intakes of Radionuclides by Workers, Publication 68, Vol. 24, no 4, Pergamon Press, 1994.
- Leggett, R.W., Reliability of the ICRP's Systemic Biokinetic Models, Radiation Protection Dosimetry, Vol. 79, 1998.
- CCSN, Normes techniques et d'assurance de la qualité des services de dosimétrie au Canada, S-106 rév 1, 2006.
- Hickey, E.E., Stoetzel, G.A., McGuire, S.A., Strom, D.J., Cicotte, G.R., Wiblin, C.M., Air Sampling in the Workplace, NUREG-1400, 1993.
- Brodsky, A., Resuspension Factors and Probabilities of Intake of Material in Process (or is 10-6 a magic number in health physics?), Health Physics, Vol. 39, No. 6, pp. 992-1000, 1980.
- noll, G.F., Radiation Detection and Measurement, John Wiley & Sons, 2000.
- CIPR, Basic Anatomical and Physiological Data for Use in Radiological Protection : Reference Values, Publication 89, 2003.
- CIPR, Recommandation 1990 de la Commission internationale de protection radiologique, Vol. 21, nos 1 à 3, Publication 60, 1991.
Renseignements Additionnels
Les documents suivants contiennent des renseignements additionnels qui pourraient présenter de l'intérêt pour les personnes participant à la conception et à la mise en œuvre d'un programme d'essai biologique :
- Commission canadienne de sûreté nucléaire, RD-58 Dépistage de l'iode radioactif déposé dans la thyroïde, juillet 2008.
- Santé et Bien-être social Canada, Bioassay Guideline 1-General Guidelines for Bioassay Programs, Direction de l'hygiène du milieu, 81-EHD-56, 1980.
- Santé et Bien-être social Canada, Bioassay Guideline 2—Guidelines for Tritium Bioassay, Rapport du Groupe fédéral-provincial sur les critères relatifs aux essais biologiques et à la surveillance in vivo, Direction de l'hygiène du milieu, 83-EHD-87, 1983.
- Leggett, R.W., Predicting the Retention of Cs in Individuals, Health Physics, Vol. 50, pp. 747-759, 1986.
- Strom, D.J., Programmes for Assessment of Dose from Intakes of Radioactive Materials, Internal Radiation Dosimetry, Health Physics 1994 Summer School, pp. 543-570, 1994.
- Commission internationale de protection radiologique, Rapport du Groupe de travail sur l'homme de référence, Publication 23, 1975.
Détails de la page
- Date de modification :